
Лауреатами Нобелевской премии по физиологии и медицине в 2018 году стали Джеймс Эллисон и Тасуку Хондзё за разработки в области терапии рака путем активации иммунного ответа. Прямая трансляция объявления победителя ведется на сайте Нобелевского комитета. Подробнее о заслугах ученых можно узнать в пресс-релизе Нобелевского комитета.
Ученые разработали принципиально новый подход к терапии рака, отличный от существовавших ранее радиотерапии и химиотерапии, который известен как «ингибирование чекпойнтов» клеток иммунитета (немного об этом механизме можно прочитать в нашем блоге, посвященном иммунотерапии). Их исследования посвящены тому, как устранить подавление активности клеток иммунной системы со стороны раковых клеток. Японский иммунолог Тасуку Хондзё (Tasuku Honjo) из университета Киото открыл рецептор PD-1 (Programmed Cell Death Protein-1) на поверхности лимфоцитов, активация которого приводит к подавлению их активности. Его американский коллега Джеймс Эллисон (James Allison) из Андерсоновского ракового центра университета Техаса впервые показал,что антитело, блокирующее ингибиторный комплекс CTLA-4 на поверхности Т-лимфоцитов, введенное в организм животных с опухолью, приводит к активации противоопухолевого ответа и уменьшению опухоли.
Исследования этих двух иммунологов привели к появлению нового класса противораковых препаратов на базе антител, связывающихся с белками на поверхности лимфоцитов, либо раковых клеток. Первый такой препарат, ипилимумаб — антитело, блокирующее CTLA-4, был одобрен в 2011 году для лечения меланомы. Антитело против PD-1, Ниволумаб, было одобрено в 2014 году против меланомы, рака легкого, почки и некоторых других типов рака.
«Раковые клетки, с одной стороны, отличаются от наших собственных, с другой стороны, являются ими. Клетки нашей иммунной системы эту раковую клетку узнают, но не убивают, — пояснил N+1 профессор Сколковского института наук и технологий и университета Ратгерса Константин Северинов. — Авторы в числе прочего открыли белок PD-1: если убрать этот белок, то иммунные клетки начинают узнавать раковые клетки и могут их убить. На этом основана терапия рака, которая сейчас широко используется даже в России. Такие препараты, ингибирующие PD-1, стали существенным компонентом современного арсенала борьбы с раком. Он очень важный, без него было бы гораздо хуже. Эти люди действительно подарили нам новый способ контроля над раком — люди живут, потому что есть вот такие терапии».
Онколог Михаил Масчан, заместитель директора Центра детской гематологии, онкологии и иммунологии имени Димы Рогачева, говорит, что иммуннотерапия стала революцией в области лечения рака.
«В клинической онкологии это одно из крупнейших событий в истории. Мы сейчас только начинаем пожинать плоды, которые принесла разработка этого типа терапии, но то, что она перевернула ситуацию в онкологии, стало ясно еще около десяти лет назад — когда появились первые клинические результаты применения лекарств, созданных на основе этих идей», — сказал Масчан в беседе с N+1.
По его словам, с помощью комбинации чекпойнт-ингибиторов долгосрочная выживаемость, то есть фактически выздоровление, может быть достигнута у 30-40 процентов пациентов с некоторыми видами опухолей, в частности, меланомой и раком легкого. Он отметил, что в ближайшем будущем появятся новые разработки, основанные на этом подходе.
«Это самое начало пути, но уже есть много видов опухолей — и рак легкого и меланома, и ряд других, при которых терапия показала эффективность, но еще больше — при которых она только исследуется, исследуются ее комбинации с обычными видами терапии. Это самое начало, и очень многообещающее начало. Число людей, которые выжили благодаря этой терапии, уже сейчас измеряется десятками тысяч», — сказал Масчан.
Каждый год в преддверие объявления лауреатов аналитики пытаются угадать, кому будет вручена премия. В этом году агентство Clarivate Analytics, которое традиционно делает прогнозы на основании цитируемости научных работ, включило в «Нобелевский список» Наполеоне Феррара, который открыл ключевой фактор формирования кровеносных сосудов, Минору Канехиса, который создал базу данных KEGG, и Саломона Снайдера, который занимался рецепторами для ключевых регуляторных молекул в нервной системе. Интересно, что Джеймса Эллисона агентство указало в качестве возможного лауреата Нобелевской премии в 2016 году, то есть в его отношении прогноз сбылся довольно скоро. Кого агентство прочит в лауреаты по остальным нобелевским дисциплинам — физике, химии и экономике, можно узнать из нашего блога «Гадаем по цитатам». По литературе в этом году премию вручать не будут.
Журналисты также предсказывали, что Нобелевский комитет отметит ученых, открывших важную роль кишечного микробиома в физиологии млекопитающих, вирусную природу рака. Самая престижная после Нобелевской премия по медицине — Ласкеровская премия, лауреаты которой нередко бывают впоследствии удостоены Нобеля — в этом году досталась Дэвиду Эллису и Майклу Грунстайну за работы в области изучения модификации гистонов (белков, связанных с ДНК), а также Джону Глену за разработку пропофола, который по сей день остается самым популярным средством для общего наркоза.
В прошлом году лауреатами Нобелевской премии по медицине и физиологии стали трое американских ученых — Джеффри Холл, Майкл Росбаш, Майкл Янг, которые были удостоены премии за открытие молекулярных механизмов, лежащих в основе работы биологических часов. Подробнее об этом можно прочитать в нашем материале «Ход часов лишь однозвучный».
Дарья Спасская
Первая в этом году Нобелевская премия по медицине-2018 была обнародована Нобелевским Комитетом 1 октября 2018 года на своем официальном сайте, где дан пресс-релиз события. Десятилетиями ученые пытались понять, почему клетки иммунной системы не могут справиться с раковыми клетками. Вопрос решен и ученые получили высшее признание — нобелевскую премию.
Премию получили двое ученых за исследования в области рака: они нашли способ, как заставить иммунную систему больного самой справиться с раковыми клетками. Лауреатами стали 70-летний профессор Техасского университета в Остине (США) Джеймс Эллисон и его 76-летний коллега Тасуку Хондзё из Киотского университета (Япония).
Они обнаружили два разных механизма, с помощью которых организм подавляет активность Т-лимфоцитов (иммунных клеток-убийц).
Если заблокировать эти механизмы, то Т-лимфоциты «выходят на свободу» и отправляются на битву с раковыми клетками. Это называют иммунотерапией рака, и она уже несколько лет применяется в клиниках.
Почему пишу эту статью? Хочу объяснить механизм, как можно заставить иммунитет самостоятельно уничтожить опасную опухоль.
Иммунитет состоит из разных клеток. Чтобы легче воспринимать информацию, я постараюсь обойтись минимумом специальной медицинской терминологии. Если говорить в общем, то в иммунная система — это ее активаторы (стимуляторы) и тормоза (ингибиторы). Именно баланс между ними свидетельствует об сильном иммунитете, который справится с любой болезнью.
Содержание
- Как работает иммунитет. Т-лимфоциты: клетки хелперы, киллеры, супрессоры
- Как опухоль пытается обмануть иммунную систему
- Нобелевская премия по медицине-2018: в чем суть открытия
- Какие препараты используют для иммунотерапии рака: название, стоимость
- Иммунитет без тормозов: Нобелевская премия за антитела против рака (2018)
- Повстанцы внутри организма
- Иммунный надзор
- Иммунологические тормоза
- Литература
- Нобелевская премия по медицине: за терапию рака
- Нобелевская премия по физиологии и медицине — 2018
- Нобелевскую премию по медицине дали за новый метод лечения рака. Что это за терапия? Объясняет онколог Михаил Ласков
Как работает иммунитет. Т-лимфоциты: клетки хелперы, киллеры, супрессоры
Названные клетки (хелперы, киллеры и супрессоры) относятся к Т-лимфоцитам — это тип белых кровяных клеток, каждая из которых исполняет определенную функцию.
Главное задание иммунитета — уметь распознавать свои и чужие клетки. С этим отлично справляются Т-хелперы — они идентифицируют чужака или свою поврежденную клетку и стимулируют иммунный ответ, вызывая к работе клетки Т-киллеры, клетки-фагоциты и усиленный синтез антител.
Т-киллеры — этот тип Т-лимфоцитов ключевые игроки в защите организма. Их еще называют клетки-убийцы, цитоксические лимфоциты («цито» в переводе означает «клетка», «токсические» — ядовитые). Они агрессивно реагируют на присутствие в организме неполноценных клеток (в том числе раковых) и чужеродного белка. О них поговорим чуть больше.
Своими отростками они прикасаются к объекту, а затем разрывают контакт и уходят. Своя «неполноценная» клетка или чужая, к которой прикоснулся лимфоцит, спустя некоторое время погибает.
Причина гибели — кусочки мембраны, оставленные на их поверхности Т-киллером. Кусочки мембраны вызывают сквозное отверстие в той клетке, к которой они прикоснулись, ее внутренняя среда начинает напрямую сообщаться с внешней — клеточный барьер нарушается. Обреченная клетка раздувается водой, из нее выходят белки цитоплазмы, органеллы разрушаются… Она погибает, а дальше к ней подходят фагоциты и пожирают ее остатки.
Реклама TIZERLADY
Как видим, тельца Т-киллеров обладают рецепторами, которые связываются с «чужими», маркируют их и заставляют организм отвечать на этот вызов – вырабатывать защиту или убивать вторгшихся. Но дополнительные белки, которые действуют, как усилители Т-лимфоцитов, также нужны для запуска полномасштабного иммунного ответа.
Именно Т-киллеры осуществляют агрессивный иммунный ответ при помощи усилителей — Т-хелперов.
Следующая группа клеток — Т-супрессоры («супрессия» означает «подавление»). Если Т-хелперы усиливают реакцию иммунитета, то супрессоры, наоборот, подавляют, регулируя силу иммунного ответа. Это позволяет иммунной системе с умеренной силой отвечать на раздражители, не вызывая аутоиммунных заболеваний.
Почему Т-клетки реагируют на раковые собственные клетки, будто они чужие? Общий принцип взаимодействия иммунной системы с опухолями выглядит следующим образом. В результате мутаций в клетках опухоли образуются белки, отличающиеся от «нормальных», к которым организм привык. Поэтому Т-клетки реагируют на них, как на чужеродные объекты.
Это очень упрощенная схема, доступная к пониманию людей без медицинского образования. Есть ряд других клеток, но перечисленных будет достаточно для понимания задачи иммунитета при обнаружении «чужого».
Реклама MEDICINETEASER
Как опухоль пытается обмануть иммунную систему
Опухоль — это система клеток, которые используют самые разные способы ускользнуть от иммунной системы. Они научились «притворяться» и «маскироваться». Некоторые опухолевые клетки скрывают видоизмененные белки со своей поверхности, другие уничтожают дефектные белки, третьи выделяют вещества, подавляющие работу иммунитета. И чем «злее» опухоль, тем меньше шансов у иммунной системы с ней справиться.
Клетки опухоли научились использовать молекулы белка CTLA4, чтобы избежать атаки иммунной системы. Раковые клетки начинают вырабатывать большое количество активаторов CTLA4.
Активаторы распознают «контрольные точки» и таким образом подавляют иммунитет. Активация «контрольных точек иммунитета» подавляет развитие иммунного ответа. К такой «контрольной точке» относится белок CTLA4, которого длительное время изучал Эллисон.
Ингибиторы, которые предложил использовать учёный, блокируют эти активаторы и не дают опухолевым клеткам избежать иммунной реакции. Итогом исследования учёного стала разработка препаратов-антител, ингибирующих «контрольные точки» — это его главное открытие.
Нобелевская премия по медицине-2018: в чем суть открытия
Нобелевскую премию в этом году вручают за снятие блокировки с Т-киллерных клеток. Нобелевские лауреаты 2018 года уже шесть лет помогают онкобольным в борьбе с опухолями, используя результаты своих исследований на практике. Учёные выяснили, как раковая опухоль «обманывает» иммунную систему и создали на основе своих исследований эффективную противораковую терапию — иммунотерапию.
Среди традиционных способов лечения рака наиболее распространены химио- и лучевая терапии. Существует и «естественные» методы лечения злокачественных образований, в том числе иммунотерапия. Одно из её перспективных направлений занимается использованием ингибиторов «контрольных точек иммунитета», расположенных на поверхности лимфоцитов (клеток иммунной системы).
Оба ученых-лауреата шли к открытию разными путями. Давайте рассмотрим что исследовал каждый из них и как им удалось заставить иммунитет справиться с онкологией.
Открытие доктора Джеймс Эллисон
Джеймс Эллисон сумел разблокировать иммунную систему с помощью антител против белка-тормоза. Доктор изучал действие определенного клеточного белка Т-лимфоцитов (условное название CTLA-4). Он пришел к выводу, что этот белок тормозит работу Т- киллеров.
Ученый искал пути, как разблокировать иммунною систему. Ему пришла идея разработать антитело, которое свяжет белок-тормоз и заблокирует его функцию подавления иммунной системы. Джеймс Эллисон провел ряд экспериментов с мышами, зараженными раком. Его интересовал вопрос, поможет ли блокада белка (CTLA-4) антителами освободить иммунную систему для атаки раковых клеток.
Больных раком лабораторных мышей удалось вылечить с помощью терапии антителами, которые сняли торможение иммунного ответа и разблокировали противоопухолевую активность Т-лимфоцитов.
В 2010 году доктор Эллисон провел клинические исследования пациентов, больных меланомой (рак кожи). У части больных полностью исчезли остаточные следы рака кожи — как следствие иммунотерапии.
Вот так это выглядит на инфографике, созданной Нобелевским комитетом.
Иммунная система начнет активно уничтожать «чужие» клетки, если будет активирован Т-лимфоцит. Для его активации необходимо связаться клеточным рецептором с другими иммунными элементами, идентифицирующими «чужого» — антигенами. Теперь должен появиться клеточный усилитель иммунного ответа, но он заблокирован белком CTLA-4. Разблокировать его можно антителами против CTLA-4.
Слева на рисунке видно белок-тормоз и клеточный рецептор. Усилитель не работает (зеленый пупырышек).
Справа — антитела (зеленого цвета) против CTLA-4 блокируют функцию торможения лимфоцитов, белок-тормоз нейтрализован антителом, клеточный усилитель подает усиленный сигнал иммунной системе и Т-лимфоциты начинают атаковать раковые клетки.
Молекула белка CTLA-4 появлялась только на активированных Т-клетках. Заслуга Эллисона в том, что он предположил, что все наоборот: CTLA-4 появляется на активированных клетках специально, чтобы их можно было остановить.
То есть, на каждой активированной Т-клетке есть ингибирующая молекула, которая конкурирует за прием сигнала (и включение или выключение работы иммунитета). Немного выше рассматривалось, как сигнал «чужой» клетки Т-хелперы передают Т-киллерам — и после приема сигнала клетки-киллеры поражают чужеродные. Но молекула белка CTLA-4 перехватывает сигнал «чужой» и блокирует киллеров.
Ученый сумел антителами связать белок-ингибитор и освободить иммунную систему для атаки раковых клеток.
Открытие доктора Тасуку Хондзё
Доктор Тасуку Хондзё на несколько лет раньше также открыл белок-тормоз (PD-1 ), расположенный на поверхности клеток лимфоцитов.
Хондзё исследовал аналогичный белок иммунных клеток (PD1) и выяснил, что он работает как тормоз, сдерживая развитие опухоли и, одновременно, блокируя Т-киллеры.
Ученый также синтезировал антитела к PD-1, которые сняли блокировку и, как результат — усиленная иммунная атака на раковые клетки.
Как видите, одновременно оба ученые сделали открытие, как снять механизм торможения протеинами работы иммунной системы. После блокировки этих белков-тормозов антителами (к каждому конкретному протеину), развязываются руки иммунным клеткам и они активно убивают онкологические опухоли.
Обе блокирующие молекулы — CTLA-4 и PD-1 — и соответствующие им сигнальные пути назвали иммунными чекпоинтами (от англ. checkpoint — контрольная точка).
В настоящее время проводится множество тестов и клинических опытов в области иммунотерапии рака и в качестве цели тестируются новые контрольные белки, обнаруженные нобелевскими лауреатами.
Прошло не меньше 15 лет между открытиями чекпоинтов и одобрением лекарств на основе их ингибиторов. Сейчас применяют шесть таких препаратов: один блокатор CTLA-4 и пять блокаторов PD-1. Почему блокаторы PD-1 оказались удачнее? Дело в том, что клетки многих опухолей тоже несут на своей поверхности PD-L1, чтобы блокировать активность Т-клеток. Таким образом, CTLA-4 активирует Т-киллеры в целом, а PD-L1 более специфично действуют на опухоль. И осложнений в случае блокаторов PD-1 возникает несколько меньше.
Источник
Какие препараты используют для иммунотерапии рака: название, стоимость
В нашей стране используют препараты для иммунной терапии онкологических опухолей. Большинство из них недоступны по цене для обычных больных.
К ним относятся:
- пембролизумаб (“Китруда”) — эффективен при раке легкого, меланоме
- ниволумаб (“Опдиво”) — эффективен при раке почки, меланоме
- ипилимумаб (“Ервой”)
- атезолизумаб (“Тецентрик”)
Препарат Китруда — представитель группы моноклональных антител. Его особенностью является возможность получения благоприятных результатов даже при лечении метастатических форм злокачественных опухолей. Несмотря на то что в России Кейтруда зарегистрирован в конце 2016 года, купить его практически не возможно даже в Москве и Санкт-Петербурге. Наши сограждане заказывают лекарство в странах Европы — Бельгии, Германии.
Стоимость одного флакона Кейтруда составляет 3290 евро.
Опдиво — более дешевый аналог Китруды.
Препарат Ервой. В качестве монотерапии назначают взрослым и детям старше 12 лет в дозе 3 мг/кг. Ервой вводят внутривенно на протяжении полутора часов каждые 3 недели в количестве четырех доз на курс лечения. Только по окончании терапии можно оценивать эффективность средства и ответную реакцию пациента.
Цена одного флакона препарата Ервой зависит от дозировки действующего вещества и составляет 4200 — 4500 евро за флакон 50 мг/10 мл и 14900 — 15 000 евро за флакон 200 мг/40 мл.
Тецентрик — препарат для терапии уротелиального рака, а также немелкоклеточного рака легких. Препарат можно купить не везде. Приобрести его можно в специализированных аптеках США, в Ватикане, в некоторых аптеках Германии, а также под заказ он поставляется в Израиль. Атезолизумаб является моноклональным антителом, специфичным к белку PD-L1.
Стоимость его – различная, в зависимости от того, где вы его приобретаете и через какую цепочку посредников он вам достался, составляет от 6,5 до 8 тыс. долларов США за один флакон.
Как видите, цена лечения не каждому по карману. Будем надеяться, что со временем, антитела против рака станут более доступными.
Врачи-иммунологи-онкологи отмечают наличие побочных эффектов в виде аутоиммунных реакций организма, которые часто проходят после прекращения лечения.
Как итог статьи. За внедрение своих разработок в лечение больных раком Нобелевская премия по медицине-2018 присуждена Нобелевским лауреатам 2018 года: Джеймс Эллисон (James Patrick Allison) и Тасуку Хондзё (Tasuku Honjo). Оба ученые сделали открытие, как снять механизм торможения протеинами работы иммунной системы и помочь иммунным клеткам расправиться с опухолью.
Кстати, недавно была опубликована еще одна статья по теме онкологии — применение амигдамина (витамин B17) для избавления от раковых клеток.
Посмотрите объяснения к открытию Нобелевских лауреатов в этом видео:
Прошу читателей: если статья понравилась — поделитесь информацией в соц. сетях — многие могут искать подобную информацию.
Будьте здоровы и берегите собственный иммунитет — тогда рак вас не коснется!
Иммунитет без тормозов: Нобелевская премия за антитела против рака (2018)
Нобелевскую премию 2018 года вручили за открытия, позволившие разработать принципиально новый подход в иммунотерапии рака, совершивший прорыв в лечении некоторых ранее смертельных опухолей. Сегодня «Биомолекула» снова расскажет об антителах-ингибиторах иммунологических чекпоинтов и о работах лауреатов этого года — Джеймса П. Эллисона и Тасуку Хондзё.
Повстанцы внутри организма
Рак — это большая группа заболеваний, объединенных общей чертой: все они начинаются с одной клетки, мутации в которой позволяют ей неограниченно делиться и формировать огромные сложно организованные скопления клеток — опухоли. Ежегодно рак убивает миллионы людей, занимая почетное второе место среди причин смерти, сразу после сердечно-сосудистых заболеваний.
С точки зрения медицины, раковые опухоли представляют собой таких же паразитов, как болезнетворные бактерии или глисты. С тем лишь отличием, что раковые клетки намного более похожи на здоровые, нежели бактерии или вирусы, да и располагаться могут в любой части тела. Но задача и там и там одна — полностью избавить организм от причины заболевания, уничтожить ее. До недавнего времени врачи располагали лишь тремя инструментами для борьбы с раком — операция, облучение ионизирующей радиацией и химиотерапия (специальные яды, бьющие по быстро делящимся клеткам). Нобелевская премия этого года дана за важнейшие шаги в разработке четвертого способа борьбы — уничтожения опухолей с помощью иммунных клеток самого пациента.
Иммунный надзор
Идею, что иммунитет и рак могут быть как-то связаны, высказал еще отец-основатель иммунологии и Нобелевский лауреат 1908 года Пауль Эрлих. Этот исследователь предположил, что опухолевые клетки могут возникать в организме постоянно, но иммунитет блокирует их развитие , . Его идеи отчасти подтвердились в 1950-х годах, когда оказалось, что переливание крови от пациентов, у которых меланома (рак кожи) ранее спонтанно исчезла, может спровоцировать такую же регрессию у пациента, получившего кровь. Исследователи пошли дальше и попробовали пересадить меланому между двумя пациентами, чем добились регрессии опухолей у обоих. Со временем идеи Эрлиха легли в основу целой теории иммунного надзора над опухолью.
Эти данные позволили разработать первую иммунотерапию рака. Подкожное введение бациллы Кальметта—Герена, сильного неспецифического иммуностимулятора, приводило к регрессии опухоли . Введением пациентам вакцин на основе стрептококка и занимался «отец иммунотерапии рака» Уильям Коли. Его результаты подтвердили предположение Эрлиха о важной роли иммунитета в подавлении развития опухолей. Однако до поры это не вылилось в серьезные медицинские прорывы.
Чтобы совершить качественный рывок в лечении рака, исследователям пришлось потратить еще несколько десятилетий на раскрытие природы иммунной защиты от опухолей. В настоящий момент эта тема изучена очень хорошо. Взаимодействие опухоли и иммунной системы устроено очень сложно. Все клетки нашего организма подвергаются постоянному иммунному надзору. Эта слежка позволяет на ранних этапах опознать раковые опухоли и задушить их в зародыше.
Для того чтобы стать раковой, клетке необходимо накопить некоторое количество мутаций в своих генах. Одни гены должны активироваться и начать стимулировать деление (их еще называют онкогенами), другие, подавляющие деление клетки (гены-супрессоры), — выключиться. При этом внутри клетки появляются измененные этими и последующими мутациями белки — неоантигены. Этот термин пришел к нам из иммунологии, где антигеном называют мишень иммунных клеток.
Дело в том, что практически все клетки нашего тела в обязательном порядке сообщают иммунитету обо всех белках, которые они содержат. Этот «иммунологический паспорт» расположен на поверхности клеток и состоит из белков главного комплекса гистосовместимости (MHC), в которых как в тисках зажаты небольшие аминокислотные цепочки — пептиды. Эти фрагменты вырезаются из всех белков, присутствующих внутри данной клетки. Специальные клетки — Т-киллеры, постоянно «ощупывают» эти белковые комплексы и когда клетка начинает производить что-то странное, убивают ее. Поэтому практически все опухоли так или иначе умеют контролировать иммунный ответ и избегать его (рис. 1).
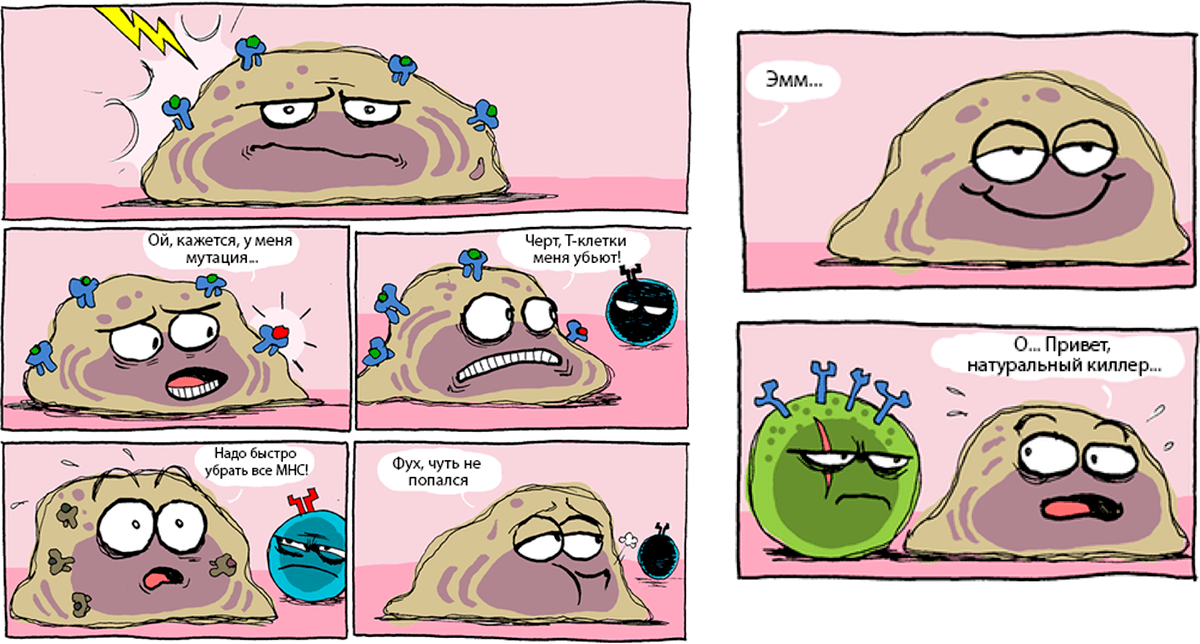
Рисунок 1. Схематическое изображение взаимодействия опухолевых клеток и иммунитета. Искаженный «иммунологический паспорт», состоящий из комплексов MHC и пептидов привлекает Т-киллеры, а его отсутствие — NK-клетки.
«Фейсбук»
Иммунологические тормоза
При той всеобъемлющей защите, которую обеспечивает нам иммунитет, кажется невероятным, что какие-то опухоли все-таки могут развиваться в организме. Особенно подобные меланоме (рис. 2), которая выделяется среди опухолей наиболее сильным искажением «иммунологического паспорта». Многие опухоли просто «набиты» иммунными клетками (рис. 3), которые почему-то их не атакуют. Должны существовать механизмы, позволяющие таким новообразованиям избегать иммунного надзора.
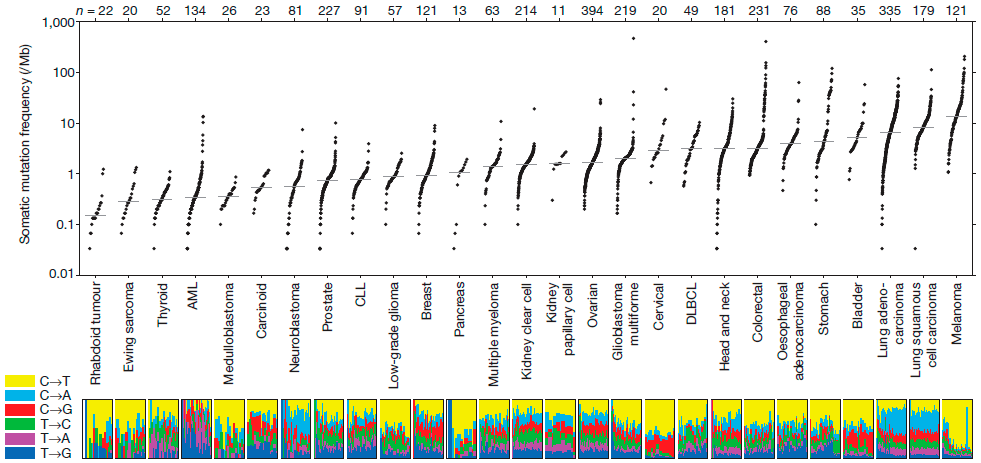
Рисунок 2. Количество мутаций в различных типах опухолей на миллион оснований ДНК. Косвенно может указывать на иммуногенность опухоли.
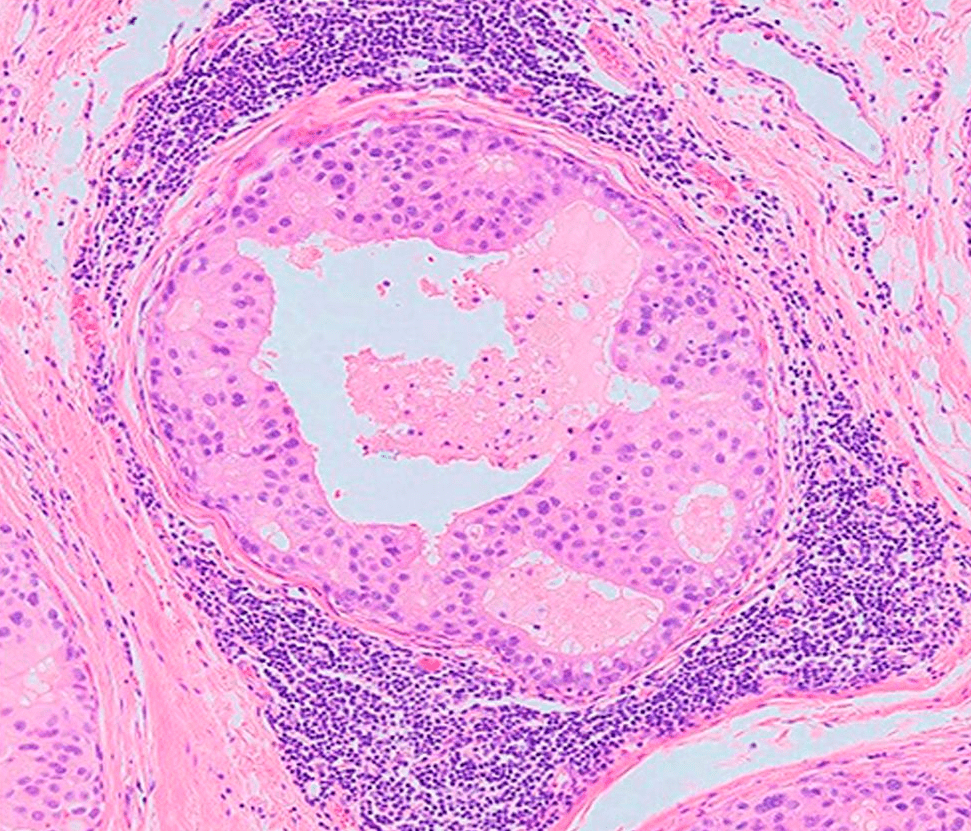
Рисунок 3. Лимфоциты (темно-фиолетовые), окружающие опухоль (в центре). Гистологический срез опухоли молочной железы.
Именно их изучением занимались лауреаты Нобелевской премии по физиологии и медицине 2018 года (рис. 4) . В 1990-х годах первый из двух лауреатов, Джеймс Эллисон, занимался изучением белка CTLA-4, который располагается на поверхности различных групп Т-лимфоцитов. Он и его коллеги заметили, что этот белок способен подавлять иммунную реакцию . Основными носителями этого белка в организме являются регуляторные Т-клетки, которые с его помощью предотвращают активацию других лимфоцитов, блокируя работу антигенпрезентирующих клеток в лимфоузлах и тканях . Эта блокировка действует как тормоз для иммунной реакции и является важной защитой от аутоиммунных заболеваний. Если же заблокировать CTLA-4, Т-лимфоциты начинают работать намного активнее.
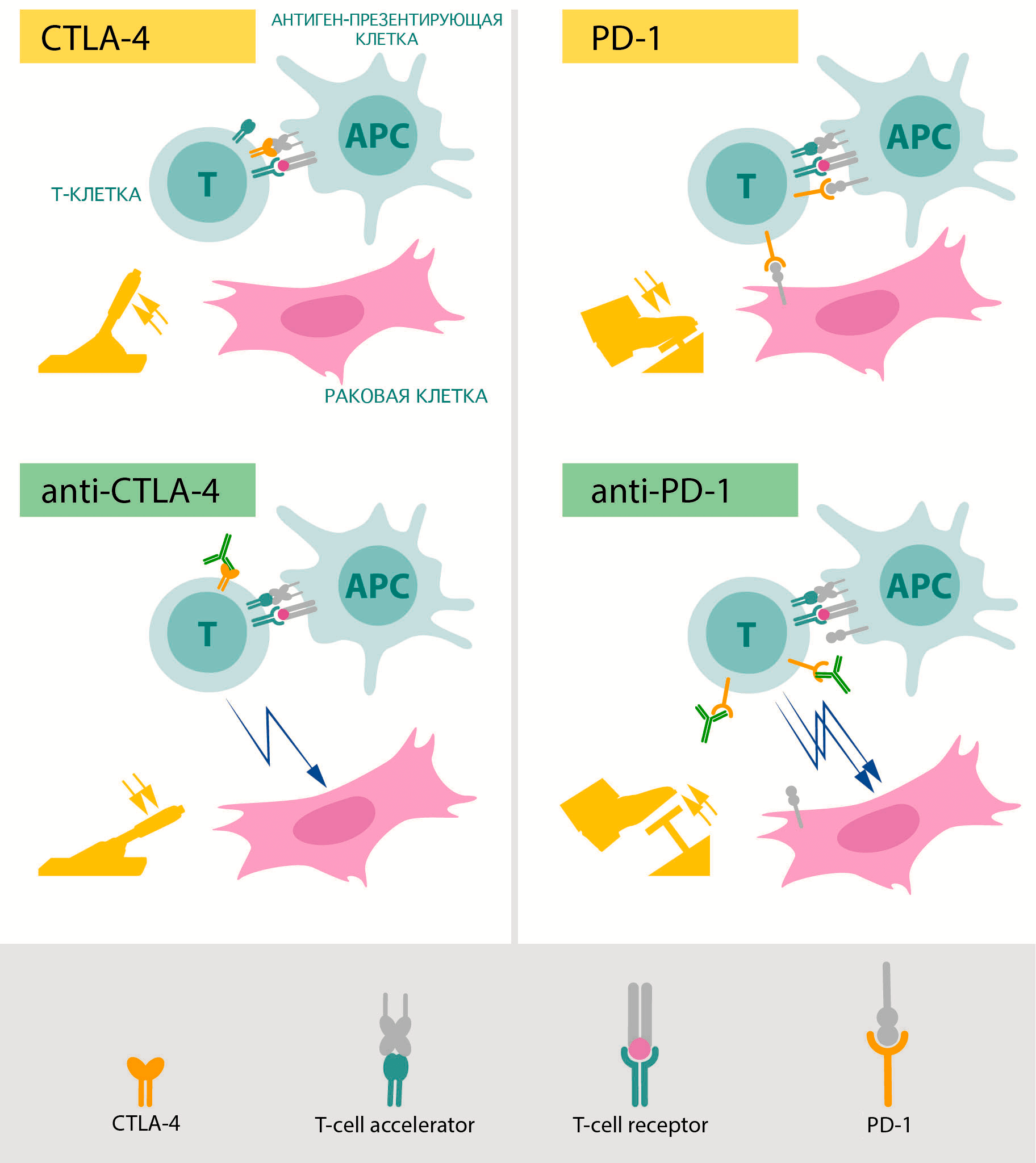
Рисунок 4. Схематическое изображение механизмов работы препаратов, разработанных на основе открытий Эллисона (слева) и Хондзё (справа). Зеленым показаны блокирующие антитела, «снимающие тормоза» с противоракового иммунитета.
Пока коллеги Эллисона изучали возможности применения знаний о CTLA-4 в терапии аллергий, ему пришло в голову, что гиперактивация этого белка может быть частью защиты опухолей от иммунитета. Его группа попробовала ввести блокирующие функцию CTLA-4 антитела мышам с развитыми формами рака и увидела серьезное снижение активности опухолевых клеток и уменьшение объема опухолевой ткани . Поначалу фармакологические компании не заинтересовались этим открытием, однако впоследствии настойчивость Эллисона, продолжившего исследования на людях, принесла свои плоды. В настоящий момент терапия антителами против CTLA-4 с использованием открытого Эллисоном механизма зарегистрирована по всему миру, в том числе и в России. Международное непатентованное название препарата — ипилимумаб . Применяют его сейчас для лечения меланомы в последней стадии, которая ранее была смертным приговором. Этот препарат также тестируется и против других форм рака.
В то время, когда группа Эллисона работала над CTLA-4 в США, в Киото исследователи под руководством профессора Тасуку Хондзё изучали другой механизм подавления иммунного ответа . Они обнаружили белок под названием PD-1, который появляется на активированных Т-киллерах . В норме этот белок позволяет регуляторным Т-клеткам подавлять те Т-киллеры, которые активировались на «неправильный» антиген. Дело в том, что активация этого белка на лимфоцитах (с помощью лиганда PD-1 — PD-L1) отправляет их в апоптоз. Именно благодаря этому он и получил свое название: PD расшифровывается как programmed death, «программируемая смерть».
В исследованиях на мышах группа Хондзё показала эффективность блокировки нового белка в борьбе с различными опухолями . Эти данные были использованы для разработки нового препарата под названием ниволумаб, который также зарегистрирован по всему миру и используется для лечения многих опухолей, в том числе и меланомы .
Так, более 100 лет спустя после первого, пророческого заявления Пауля Эрлиха, иммунитет наконец-то стал надежным союзником человека в борьбе с онкологическими заболеваниями.
Литература
Нобелевская премия по медицине: за терапию рака
Иммунная система человека вынуждена поддерживать баланс: она распознает и атакует все чужеродные для организма белки, однако не трогает собственные клетки тела. Этот баланс особенно тонок в случае раковых клеток: генетически они не отличаются от здоровых клеток тела. Функция белка CTLA4, c которым работал Джеймс Эллисон, состоит в том, чтобы служить контрольной точкой иммунного ответа и не позволять иммунной системе атаковать собственные белки. Белок PD1, предмет научных интересов Тасуку Хондзё — компонент системы «программируемой клеточной смерти». Его функции также состоять в том, чтобы не допустить аутоиммунной реакции, но действует он иным путем: запускает или контролирует механизм клеточной смерти Т-лимфоцитов.
Иммунотерапия рака — одно из самых перспективных направлений современной онкологии. Оно основано на том, чтобы подтолкнуть иммунную систему пациента к распознаванию и уничтожению клеток злокачественных опухолей. Научные открытия нобелевских лауреатов этого года легли в основу высокоэффективных противоопухолевых препаратов, уже одобренных к применению. В частности, препарат «Кейтруда» атакует белок PD1, рецептор запрограммированной клеточной гибели. Препарат одобрен к применению в 2014 году и применяется для лечения немелкоклеточного рака легких и меланомы. Другой препарат, «Ипилимумаб», атакует белок CTLA4 — тот самый «тормоз» иммунной системы — и тем самым активирует ее. Это средство применяется у пациентов с раком легкого или простаты на поздних стадиях, и больше чем в половине случаев позволяет остановить дальнейший рост опухоли.
Джеймс Эллисон и Тасуку Хондзё стали 109-м и 110-м лауреатами Нобелевской премии по медицине, которая присуждается с 1901 года. Среди лауреатов прежних лет двое российских ученых: Иван Павлов (1904) и Илья Мечников (1908). Интересно, что Илья Мечников получил свою премию с формулировкой «За труды по иммунитету», то есть за достижения в той же области биологической науки, что и лауреаты 2018 года.
Нобелевская премия по физиологии и медицине — 2018

Рис. 1. Нобелевские лауреаты 2018 года: Джеймс Эллисон (James Patrick Allison) и Тасуку Хондзё (Tasuku Honjo). Фото с сайтов chron.com и asahi.com
В 2018 году лауреатами Нобелевской премии по физиологии и медицине стали двое ученых с разных концов света — Джеймс Эллисон из США и Тасуку Хондзё из Японии, — независимо открывшие и изучавшие один и тот же феномен. Они обнаружили два разных чекпоинта — механизма, с помощью которых организм подавляет активность Т-лимфоцитов, иммунных клеток-убийц. Если заблокировать эти механизмы, то Т-лимфоциты «выходят на свободу» и отправляются на битву с раковыми клетками. Это называют иммунотерапией рака, и она уже несколько лет применяется в клиниках.
Нобелевский комитет любит иммунологов: по меньшей мере каждая десятая премия по физиологии и медицине вручается за теоретические иммунологические работы. В этом же году речь зашла о практических достижениях. Нобелевские лауреаты 2018 года отмечены не столько за теоретические открытия, сколько за последствия этих открытий, которые уже шесть лет помогают онкобольным в борьбе с опухолями.
Общий принцип взаимодействия иммунной системы с опухолями выглядит следующим образом. В результате мутаций в клетках опухоли образуются белки, отличающиеся от «нормальных», к которым организм привык. Поэтому Т-клетки реагируют на них как на чужеродные объекты. В этом им помогают дендритные клетки — клетки-шпионы, которые ползают по тканям организма (за их открытие, кстати, присудили Нобелевскую премию в 2011 году). Они поглощают все проплывающие мимо белки, расщепляют их и выставляют получившиеся кусочки на свою поверхность в составе белкового комплекса MHC II (главный комплекс гистосовместимости, подробнее см.: Кобылы определяют, беременеть или нет, по главному комплексу гистосовместимости… соседа, «Элементы», 15.01.2018). С таким багажом дендритные клетки отправляются в ближайший лимфатический узел, где показывают (презентируют) эти кусочки пойманных белков Т-лимфоцитам. Если Т-киллер (цитотоксический лимфоцит, или лимфоцит-убийца) узнает эти белки-антигены своим рецептором, то он активируется — начинает размножаться, образуя клоны. Дальше клетки клона разбегаются по организму в поисках клеток-мишеней. На поверхности каждой клетки организма есть белковые комплексы MHC I, в которых висят кусочки внутриклеточных белков. Т-киллер ищет молекулу MHC I с антигеном-мишенью, который он может распознать своим рецептором. И как только распознавание произошло, Т-киллер убивает клетку-мишень, проделывая дырки в ее мембране и запуская в ней апоптоз (программу гибели).

Рис. 2. Тасуку Хондзё в окружении своих коллег по лаборатории. Фото с сайта asianscientist.com
Но этот механизм не всегда работает эффективно. Опухоль — это гетерогенная система клеток, которые используют самые разные способы ускользнуть от иммунной системы (об одном из недавно открытых таких способов читайте в новости Раковые клетки повышают свое разнообразие, сливаясь с иммунными клетками, «Элементы», 14.09.2018). Некоторые опухолевые клетки скрывают белки MHC со своей поверхности, другие уничтожают дефектные белки, третьи выделяют вещества, подавляющие работу иммунитета. И чем «злее» опухоль, тем меньше шансов у иммунной системы с ней справиться.

Рис. 3. Джеймс Эллисон с фигурками участников музыкальной группы The Checkpoints, в которой он играет вместе со своими коллегами, названной в честь иммунных чекпоинтов, за открытие которых и присуждена Нобелевская премия. Фото с сайта houstonchronicle.com
Классические методы борьбы с опухолью предполагают разные способы убийства ее клеток. Но как отличить опухолевые клетки от здоровых? Обычно используют критерии «активное деление» (раковые клетки делятся гораздо интенсивнее большинства здоровых клеток организма, и на это нацелена лучевая терапия, повреждающая ДНК и препятствующая делению) или «устойчивость к апоптозу» (с этим помогает бороться химиотерапия). При таком лечении страдают многие здоровые клетки, например стволовые, и не затрагиваются малоактивные раковые клетки, например спящие (см.: Удалось выяснить, почему рак может уснуть и проснуться через много лет, «Элементы», 10.06.2016). Поэтому сейчас часто делают ставку на иммунотерапию, то есть активацию собственного иммунитета больного, так как иммунная система лучше, чем внешние лекарства, отличает опухолевую клетку от здоровой. Активировать иммунную систему можно самыми разными способами. Например, можно забрать кусочек опухоли, выработать антитела к ее белкам и ввести их в организм, чтобы иммунная система лучше «видела» опухоль. Или же забрать иммунные клетки и «натаскать» их на распознавание специфических белков. Но Нобелевскую премию в этом году вручают за совсем другой механизм — за снятие блокировки с Т-киллерных клеток.
Когда эта история только начиналась, никто не думал об иммунотерапии. Ученые пытались разгадать принцип взаимодействия Т-клеток с дендритными клетками. При ближайшем рассмотрении оказывается, что в их «общении» участвуют не только MHC II c белком-антигеном и рецептор Т-клетки. Рядом с ними на поверхности клеток расположены и другие молекулы, которые тоже участвуют во взаимодействии. Вся эта конструкция — множество белков на мембранах, которые соединяются друг с другом при встрече двух клеток, — называется иммунным синапсом (см. Immunological synapse). В состав этого синапса входят, например, костимулирующие молекулы (см. Co-stimulation) — те самые, которые посылают сигнал Т-киллерам активироваться и отправляться на поиски врага. Их обнаружили первыми: это рецептор CD28 на поверхности Т-клетки и его лиганд В7 (CD80) на поверхности дендритной-клетки (рис. 4).

Рис. 4. Иммунный синапс при взаимодействии Т-клетки и дендритной клетки. Слева — дендритная клетка, справа — Т-клетка. Видны два взаимодействия: распознавание антигена (MHC + Т-клеточный рецептор) и костимуляция (B7 + CD28). В Т-клетке костимуляция улучшает выживание, стимулирует деление, вызывает транскрипцию новых генов и секрецию новых белков на поверхность клетки (см.: Co-stimulation). Рисунок из статьи A. K. S. Salama, F. S. Hodi, 2011. Cytotoxic T-Lymphocyte–Associated Antigen-4
Джеймс Эллисон и Тасуку Хондзё независимо обнаружили еще две возможные составляющие иммунного синапса — две ингибирующие молекулы. Эллисон занимался открытой в 1987 году молекулой CTLA-4 (cytotoxic T-lymphocyte antigen-4, см.: J.-F. Brunet et al., 1987. A new member of the immunoglobulin superfamily — CTLA-4). Изначально считалось, что это еще один костимулятор, потому что она появлялась только на активированных Т-клетках. Заслуга Эллисона в том, что он предположил, что всё наоборот: CTLA-4 появляется на активированных клетках специально, чтобы их можно было остановить! (M. F. Krummel, J. P. Allison, 1995. CD28 and CTLA-4 have opposing effects on the response of T cells to stimulation). Дальше оказалось, что CTLA-4 похожа по структуре на CD28 и тоже может связываться с B7 на поверхности дендритных клеток, причем даже сильнее, чем CD28. То есть на каждой активированной Т-клетке есть ингибирующая молекула, которая конкурирует с активирующей молекулой за прием сигнала. А поскольку в состав иммунного синапса входит множество молекул, то результат определяется соотношением сигналов — тем, сколько молекул CD28 и CTLA-4 смогли связаться с B7. В зависимости от этого Т-клетка либо продолжает работу, либо замирает и не может никого атаковать.
Тасуку Хондзё обнаружил на поверхности Т-клеток другую молекулу — PD-1 (ее название — сокращение от programmed death), которая связывается с лигандом PD-L1 на поверхности дендритных клеток (Y. Ishida et al., 1992. Induced expression of PD‐1, a novel member of the immunoglobulin gene superfamily, upon programmed cell death). Оказалось, что мыши, нокаутные по гену PD-1 (лишенные соответствующего белка), заболевают чем-то похожим на системную красную волчанку. Это аутоиммунное заболевание, то есть состояние, когда иммунные клетки атакуют нормальные молекулы организма. Поэтому Хондзё заключил, что PD-1 тоже работает как блокатор, сдерживая аутоиммунную агрессию (рис. 5). Это еще одно проявление важного биологического принципа: каждый раз, когда запускается какой-либо физиологический процесс, параллельно запускается противоположный ему (например, свертывающая и противосвертывающая системы крови), чтобы избежать «перевыполнения плана», которое может оказаться губительным для организма.

Рис. 5. Иммунный синапс, подавляющий активность Т-клетки. Слева — дендритная клетка, справа — Т-клетка. В центре синапса — распознавание антигена (MHC + Т-клеточный рецептор), ниже — CD28, ни с чем не связанный. Сверху показано ингибирующее взаимодействие B7 + CTLA-4, снизу — второй ингибитор PD-L2 + PD-1. В Т-клетке заблокированы сигнальные пути от CD28, снижены выживаемость и деление. Рисунок из статьи A. K. S. Salama, F. S. Hodi, 2011. Cytotoxic T-Lymphocyte–Associated Antigen-4
Обе блокирующие молекулы — CTLA-4 и PD-1 — и соответствующие им сигнальные пути назвали иммунными чекпоинтами (от англ. checkpoint — контрольная точка, см. Immune checkpoint). По всей видимости, это аналогия с чекпоинтами клеточного цикла (см. Cell cycle checkpoint) — моментами, в которые клетка «принимает решение», может ли она продолжать делиться дальше или какие-то ее компоненты существенно повреждены.
Но на этом история не закончилась. Оба ученых решили найти применение новооткрытым молекулам. Их идея состояла в том, что можно активировать иммунные клетки, если заблокировать блокаторы. Правда, побочным эффектом неизбежно будут аутоиммунные реакции (как и происходит сейчас у пациентов, которых лечат ингибиторами чекпоинтов), зато это поможет победить опухоль. Блокировать блокаторы ученые предложили с помощью антител: связываясь с CTLA-4 и PD-1, они механически их закрывают и мешают взаимодействовать с B7 и PD-L1, при этом Т-клетка не получает ингибирующих сигналов (рис. 6).
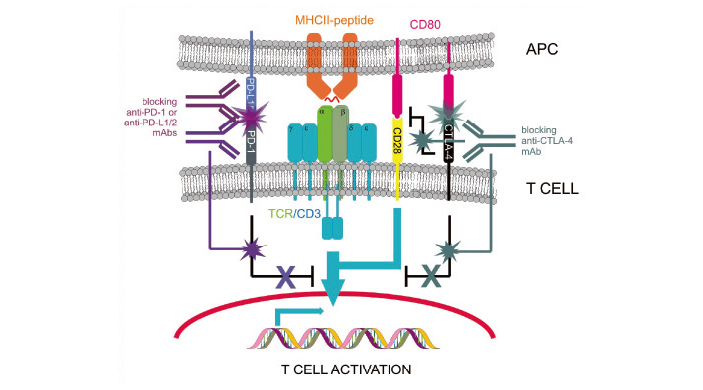
Рис. 6. Иммунный синапс с участием антител — блокаторов ингибирующих сигналов. Сверху — дендритная клетка, снизу — Т-клетка. В центре — распознавание антигена, слева от него — активирующий сигнал CD80 (B7) + CD28. Крайние правое и левое взаимодействия — ингибирующие сигналы PD-L1 + PD-1 и CD80 + CTLA-4, на которые действуют антитела. Рисунок из статьи A. Ortega-Carrion, M. Vicente-Manzanares, 2016. Concerning immune synapses: a spatiotemporal timeline
Прошло не меньше 15 лет между открытиями чекпоинтов и одобрением лекарств на основе их ингибиторов. На данный момент применяют уже шесть таких препаратов: один блокатор CTLA-4 и пять блокаторов PD-1. Почему блокаторы PD-1 оказались удачнее? Дело в том, что клетки многих опухолей тоже несут на своей поверхности PD-L1, чтобы блокировать активность Т-клеток. Таким образом, CTLA-4 активирует Т-киллеры в целом, а PD-L1 более специфично действуют на опухоль. И осложнений в случае блокаторов PD-1 возникает несколько меньше.
Современные методы иммунотерапии пока, увы, не являются панацеей. Во-первых, ингибиторы чекпоинтов всё равно не обеспечивают стопроцентной выживаемости пациентов. Во-вторых, они действуют не на все опухоли. В-третьих, их эффективность зависит от генотипа пациента: чем более разнообразны его молекулы MHC, тем выше шанс на успех (о разнообразии белков MHC см.: Разнообразие белков гистосовместимости повышает репродуктивный успех у самцов камышовок и снижает у самок, «Элементы», 29.08.2018). Тем не менее получилась красивая история о том, как теоретическое открытие сначала меняет наши представления о взаимодействии иммунных клеток, а затем рождает лекарства, которые можно применять в клинике.
А нобелевским лауреатам есть над чем работать дальше. Точные механизмы работы ингибиторов чекпоинтов всё еще не известны до конца. Например, в случае CTLA-4 так и непонятно, с какими именно клетками взаимодействует лекарство-блокатор: с самими Т-киллерами, или с дендритными-клетками, или вообще с Т-регуляторными клетками — популяцией Т-лимфоцитов, отвечающей за подавление иммунного ответа. Поэтому эта история, на самом деле, еще далека от завершения.
Полина Лосева
Нобелевскую премию по медицине дали за новый метод лечения рака. Что это за терапия? Объясняет онколог Михаил Ласков
Объявление лауреатов Нобелевской премии по медицине. 1 октября 2018 года, Стокгольм Ye Pingfan / Xinhua/ SIPA / Scanpix / LETA
В 2018 году Нобелевскую премию по медицине дали двум ученым — Джеймсу Эллисону из США и Тасуку Хондзё из Японии — они разработали новую терапию онкологических заболеваний. Мы попросили онколога Клиники амбулаторной онкологии и гематологии Михаила Ласкова объяснить, в чем суть их работы.
За что дали премию?
Коротко. За разработку препаратов, которые мешают опухолевым клеткам сопротивляться иммунной системе.
Нобелевскую премию в этом году дали за изобретение ингибиторов контрольных точек — препаратов, которые заставляют иммунитет активно уничтожать опухоль. Химиотерапия и таргетная терапия либо напрямую убивают опухолевые клетки, либо вмешиваются в их процессы, что тоже приводит к их смерти. Иммунная терапия не обладает самостоятельным противоопухолевым эффектом — она заставляет иммунные клетки убивать опухоль. В англоязычной литературе об этой терапии пишут, что она «снимает иммунитет с тормоза».
Иммунная клетка пытается съесть опухолевую или просто убить, а та старается сопротивляться — с помощью особых молекул связывается с иммунной и уговаривает ее остановиться. Иммунная терапия вмешивается в эти переговоры: она либо блокирует тормоз (определенные контрольные точки) на клетке иммунной системы, либо блокирует белки (PD-L1) на опухолевой клетке, которые позволяют уклоняться от действия иммунитета.
Правда, снятие с тормоза в ряде случаев приводит к тому, что иммунитет атакует свои собственные клетки. Это в чем-то похоже на аутоиммунные болезни, и проблема немаленькая. Частые побочные эффекты — усталость, кашель, тошнота, сыпь, зуд, потеря аппетита. Но при некоторых схемах иммунотерапии серьезные побочные эффекты (именно серьезные: диарея, воспаление кишечника, легких и так далее) могут возникать в одном случае из двух.
Какие онкологические заболевания так лечат?
Коротко. Если в опухоли есть определенные маркеры, так можно лечить рак чего угодно — желудка, легких и т. д. Пока лучшие результаты терапия показала в лечении меланомы и рака легких.
Это зависит от определенных маркеров. Иммунотерапия — это первая терапия, про которую по-английски говорят histology agnostic indications. Это значит, что если есть определенные маркеры в опухоли, то ингибиторы контрольных точек (те самые новые препараты) можно назначать вне зависимости от расположения рака. Например, если есть микросателлитная нестабильность, то можно назначать пембролизумаб («Китруду») и для глиобластомы, и для рака желудка, и для чего угодно. Другой вопрос, что она очень редко возникает в этих опухолях.
В последние несколько лет эта терапия стала прорывом. Есть заболевания, которые трудно лечить. Это глиобластома, меланома, рак легких, рак поджелудочной железы, рак желудка и так далее. Иммунотерапия позволила значительно улучшить результаты по некоторым из этих заболеваний, а именно меланоме и раку легких. Некоторые такие пациенты, по нынешним данным, могут жить несколько лет без признаков заболевания.
Но пока такая терапия используется в основном для метастатических раков. Это связано с тем, что сначала в исследованиях участвуют люди именно с тяжелыми случаями, а потом проводятся новые исследования, и показания часто расширяются на менее безнадежные ситуации. И уже сейчас такие препараты назначают, например, при третьей стадии, в качестве послеоперационной терапии при меланоме.
Такие препараты есть в России?
Коротко. Да, но не все и они очень дорогие.
К сожалению, нельзя сказать, что такие лекарства всем доступны. По одному тарифу в государственной больнице на него могут выделять 180 тысяч рублей, притом что в реальной жизни препарат будет стоить 300 и больше. То есть лекарство просто не назначат, потому что не на что покупать. С другой стороны, получить эти дорогие препараты иногда позволяет так называемая региональная льгота, которая регулируется законом о социальной помощи; такие закупки в некоторых регионах финансируются бюджетом.
Еще о лечении онкологических заболеваний
- Генная терапия — это нормальный метод лечения. Доказано В США разрешат внедрять ген, помогающий убивать злокачественные клетки больных лейкозом: The New York Times
Интервью взяла Дарья Саркисян
- Напишите нам